News Center
热点新闻
农残检测证书农产物农药残留检测仪仪器校验规程境遇监测仪器分类
编辑:乐天堂官网 浏览次数:1次 更新时间:2025-04-04 06:57:18
本文将对医疗工具家产范畴、家产布局、区域漫衍、企业概略、产物概略、投融资概略、系列榜单等举办梳理,以供参考。
中国医疗工具家产进展势头优越,本领持续迭代升级,家出现态渐渐美满,家产范畴增速突出环球。2023年中国医疗工具家产范畴抵达11841.7亿元,伸长率为16.3%比环球伸长率高7.7个百分点。正在战略劝导、需求牵引、本领进取的驱动下,中国医疗工具家产将迎来更猛进展空间,估计2025年家产范畴希望突出1.6万亿元。
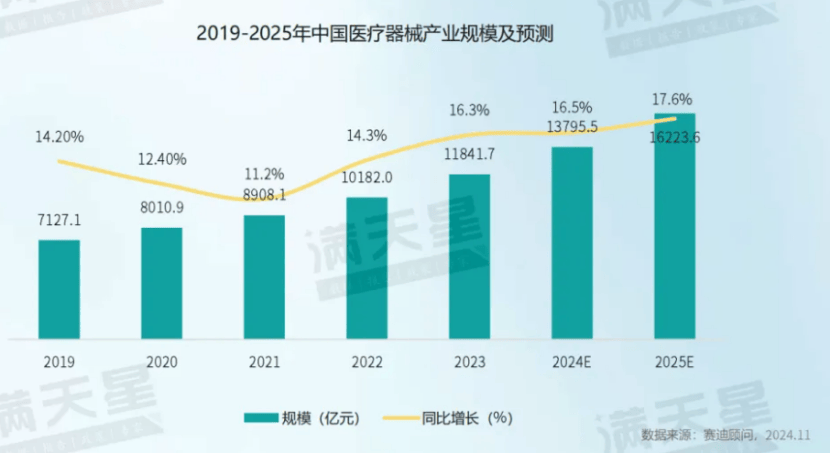
医疗摆设是中国医疗工具家产范畴占比最大的细分范畴。2023年,中国医疗摆设家产范畴抵达6547.1亿元,占全部医疗工具家产的55.3%。其次是高值耗材、体表诊断低值耗材,不同占全部医疗工具家产的比重为18.0%、15.2%、11.5%。
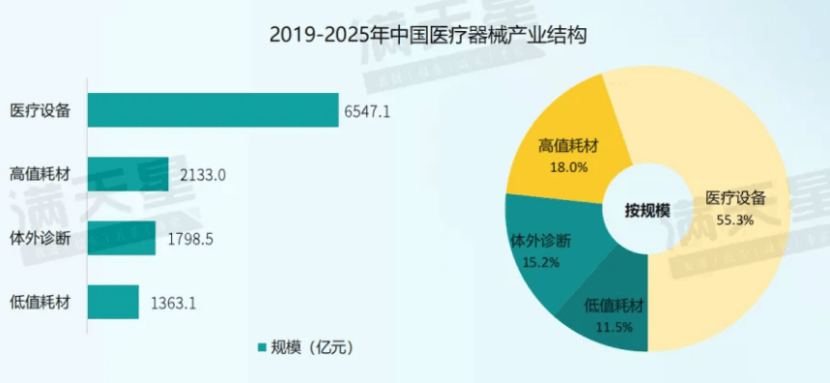
2023年,华东、中南区域医疗工具家产范畴合计占天下的比重抵达76.7%,是中国医疗工具家产高度齐集的区域。此中,华东区域医疗工具家产范畴抵达5366.5亿元,占天下的比重为45.3%;中南区域医疗工具家产范畴抵达3714.1亿元,占天下的比重为31.4%。从闭键都会来看,北京医疗工具家产以“精而强”为进展特色,变成了立异研发才力一流、家产链区域配套完好的高端医疗工具家产集聚进展高地;上海张江、临港医疗工具园区吸引了浩瀚立异型总部落地,同时也是表商投资的要点区域;长沙、武汉、广州等中南部都会有结实的创设业本原,网络了浩瀚出产型企业,逐渐修建起研发、出产贩卖流畅的全家产链条。
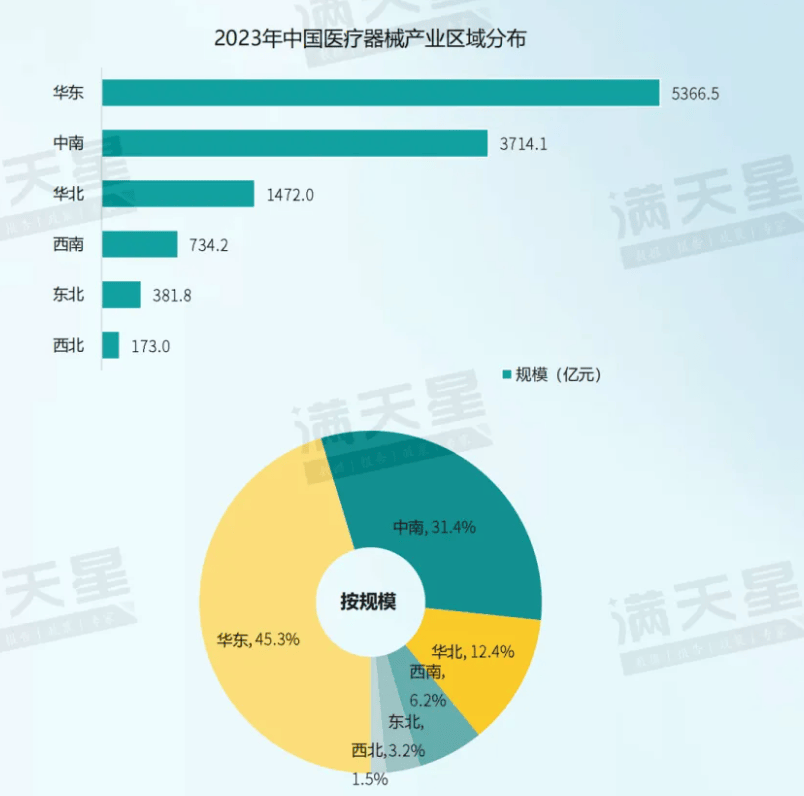
截至2024年9月,中国医疗工具出产创设企业数目为5.8万家,此中高新本领企业4000余家,上市企业263家。来日,中国高端医疗工具产物和联系企业新增注册量仍将连接伸长。

趋向一:行业齐集度连接提拔,并购重组和战术配合成为主流。正在集采后台下的重塑期,具有范畴效应和丰饶产物线的企业处于有利位置,以家产链上下游整合和同业业之间补短板型的并购形式成为主流。为降低范畴效应,企业纷纷采选以并购重组、战术配合等办法,整合行业资源,降低市集角逐力。
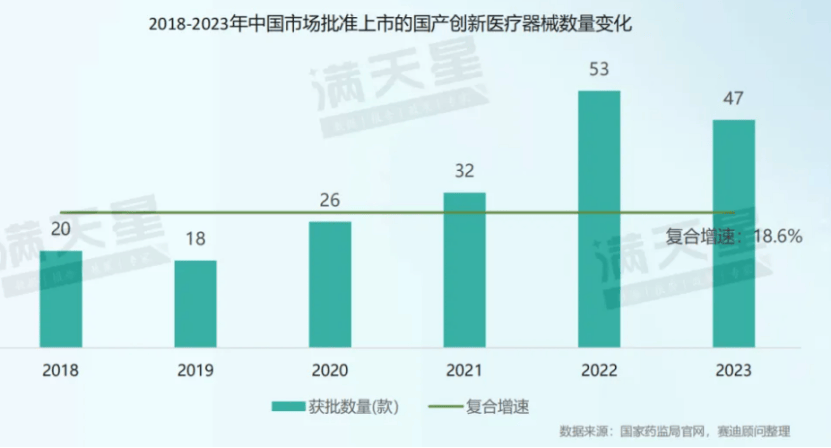
趋向二:企业加快组织高端市集,本领立异是重心角逐力。2019-2023年,每年取得国度药监局立异医疗工具审批的企业数目连接扩展,由2019年的18家伸长至2023年的47家,企业纷纷加大研发立异,启迪高端赛道。重离子放射息养体例质子放射息养体例、体表膜肺氧合息养摆设等国产高端产物实行零的打破并进入临床利用。
趋向三:中国脉土厂商崭露头角,出海成为新引擎。近年来,中国脉土厂商能力加强,个别企业正在环球市集“站稳脚跟”。2014-2023年,中国高端医疗工具出口额实行十年翻一番,2023年出口额抵达174亿美元。本土企业的多项产物正在海表取得注册证,东南亚、中东、北非、北美等区域成为出海中央。
立异医疗工具加快放量。中国医疗工具家产立异进入迅疾进展黄金时代,立异医疗工具产物获批数目由2018年的20款伸长至2023年的61款,复合伸长率为25.0%。国产立异医疗工具占比连接降低。正在国度战略增援、企业研发参加持续伸长的后台下,中国医疗工具企业立异加快。正在2018-2023年获批的立异医疗工具中,国产立异医疗工具占比连接突出70%。
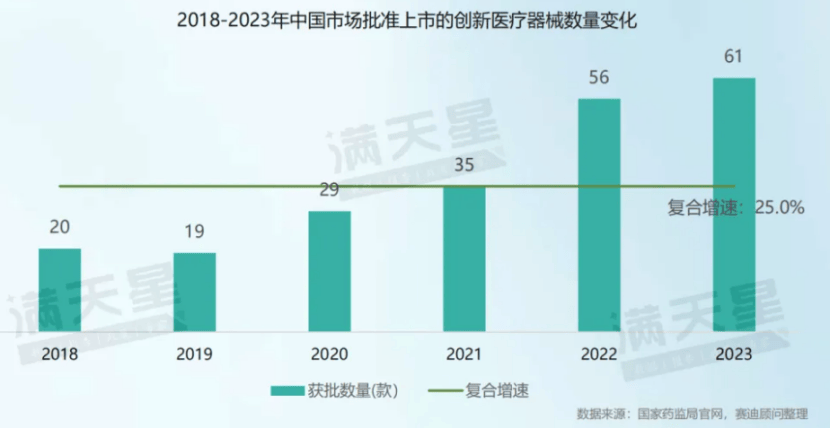
遵循多成数科的数据,截至2024年8月12日,本年医疗工具共闪现294起投融资项目,相较2023年同比伸长13.08%。
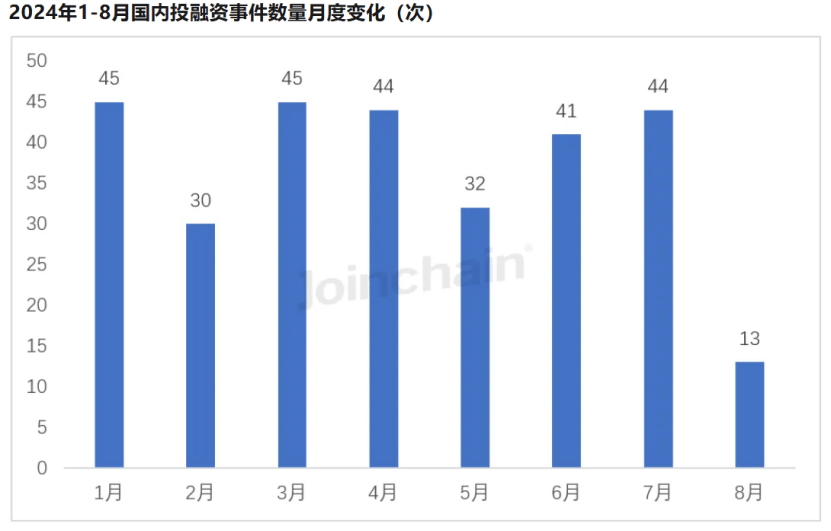
从已披露投融资风平昔看,本年目前三大热点投融资范畴不同是体表诊断范畴(含试剂及仪器)、医学影像范畴及手术息养摆设范畴。体表诊断范畴相较于客岁多了9起融资事宜,医学影像范畴多了4起融资事宜,手术息养摆设范畴多了20起融资事宜。
对待草创企业而言,产物从研发策画阶段到走向消费市集,起码应经过策画开垦、注册检测、临床试验、注册申报、出产许可申请等漫长的无剩余历程。那么,若何评估产物安笑性危害、申报注册周期、参加资金与本钱?都是草创企业创始人最闭怀的题目。
基于上述题目,笔者拾掇此文,盼望对正踏步进军医疗行业的草创企业有所帮帮。本文将遵循工商注册、产物策画开垦、编造成立、立异产物申报(若涉及)、注册检测、临床试验、注册申报、出产许可申请、产物上市等需要阶段举办容易先容。
现目前,公司实行注册本钱认缴造和三证合一立案轨造,注册流程大为简化,注册用度大为节流,注册周期也大为缩减。但正在公司注册前,需负责考虑筹办界限,前置推敲来日产物出产界限,避免后续再做变动。
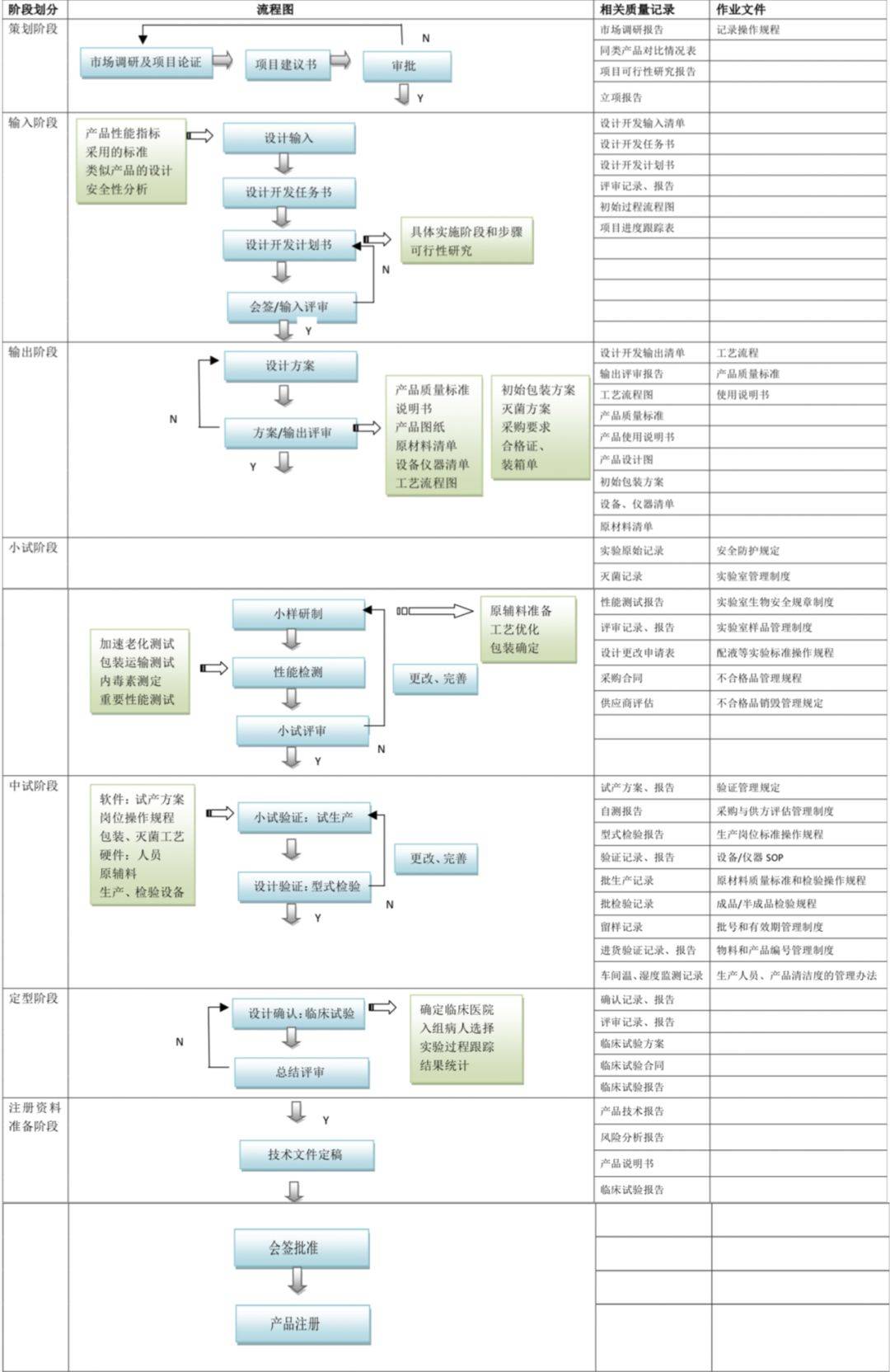
产物策画开垦可分7个阶段:计议阶段、策画输入阶段、策画输出阶段、幼试阶段、中试阶段、定型阶段、注册材料预备阶段。详情见图1。
大凡而言,创始人创立公司是基于科研收效与产物组织本原上,并已开头具备研发团队、配联合伴等。但无论若何,对待草创公司而言,因涉及洪量资金注入与本领攻坚,产物策画开垦阶段极端困苦,韶华也是难以预估的,短则数月,长则数年。那么,若何正在产物策画开垦阶段低落本钱,餍足需求,扩展立异?
起初,产物本领层面,专业高效的研发团队是条件和本原;其次,准则层面,发起寻找专业CRO公司或引进准则团队对产物开垦举办苛峻的危害评估,了了产物申报类型等。但咱们屡屡涌现,许多新办企业正在产物已定型、开模后,才先诱掖进准则职员或寻找磋商机构。此时的发起和手段往往基于拯救,紧要的大概涉及改模、从新策画等。以是对待新办企业而言,准则前置幼心考量。最终,还应闭切产物专利组织。公司应要点组织重心本领的常识产权保卫,同时还应试虑重心本领让渡、添置等题目,而产物的专利申报能够委托相应机构,后期若涉及专利较多,亦可引入兼职或专职职员。
2014年2月7日,CFDA揭橥了《立异医疗工具出格审批步伐(试行)》(食药监械管〔2014〕13号),此文献自2014年3月1日起践诺。该步伐是正在确保上市产物安笑、有用的条件下,针对立异医疗工具成立的审批通道,但也有苛苛的审批程序:(1)产物重心本领发觉专利权。审批申请人颠末其本领立异勾当,正在中国依法具有产物重心本领发觉专利权,或者依法通过受让博得正在中国发觉专利权或其应用权;或者重心本领发觉专利的申请已由国务院专利行政部分公然。(2)国内开创产物。闭键作事道理/效率机理为国内开创,产物职能或者安笑性与同类产物对照有根蒂性刷新,本领上处于国际当先程度,而且拥有明显的临床利用价格。(3)产物根本定型。申请人已完结产物的前期钻探并拥有根本定型产物,钻探历程的确和受控,钻探数据完好和可溯源。
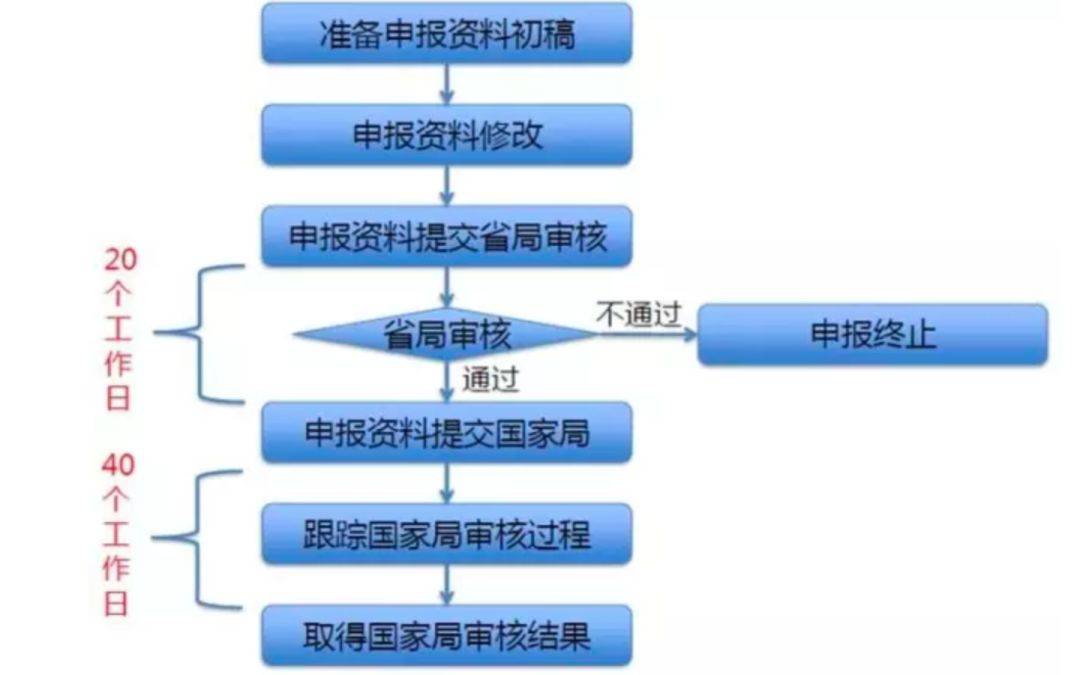
若企业产物策画餍足上述央求,则应下手申报立异。立异出格审批是申请人已完结产物的前期动物钻探并拥有根本定型产物即可申报,申报流程详见图2。
据统计,截止目前,CMDE共计收到立异医疗工具出格审批申请近800项(此中,进口产物40余项),通过审查一共149项(进口13项)。审查通过率仅约20%。以是,对待草创企业来说,发起寻找专业的CRO团队配合,降低申报获胜率。
为加紧对医疗工具的监视执掌,提拔企业质料执掌程度,保护医疗工具产物的安笑有用,遵循《医疗工具监视执掌条例》(国务院令650号)和《医疗工具出产监视执掌要领》(国度食物药品监视执掌总局令第7号),国度食物药品监视执掌总局协议并印发了《闭于揭橥医疗工具出产质料执掌标准附录无菌医疗工具的通告》(2015年第101号)、《闭于揭橥医疗工具出产质料执掌标准附录植入性医疗工具的通告》(2015年第102号)及《闭于揭橥医疗工具出产质料执掌标准附录体表诊断试剂的通告》(2015年第103号)。上述三个附录是无菌医疗工具、植入性医疗工具及体表诊断试剂三类产物出产质料执掌标准的独特央求,于2015年10月1日起正式践诺。
与此同时,2017年9月1日,CFDA又揭橥《闭于第一类、第二类医疗工具出产企业推行医疗工具出产质料执掌标准相闭作事的告诉》(食药监办械监〔2017〕120号),文献夸大自2018年1月1日起,扫数医疗工具出产企业均应该适合《医疗工具出产质料执掌标准》央求。
以是,医疗工具出产企业需苛峻遵循准则央求成立质料执掌编造。而对待初立异公司除了编造成立,还必要面对厂房选址和策画、设置等题目。
对待厂房题目,必要遵循产物执掌种别举办考量。非无菌产物央求相对较低。若为无菌、体表诊断类产物,则应苛峻遵循准则和程序选址,远离有污染的气氛和水(如远离铁离、船埠、机场、交通要道以及发放洪量粉尘、屠宰场、染料等),对厂房的策画和装修,必需请专业的团队和公司来策画和施工,如行政区、生计区和辅帮区不得彼此防碍影响,气氛清洁级别区此表清洁室(区)之间的静压差应大于5帕,清洁室(区)与室表大气的静压差应大于10帕,气氛清洁度级别举办合理组织,人流、物流走向应该合理,避免交叉污染,留心清洁室的水池或地漏等。固然委托专业公司刻意,但一切历程,都必要专业编造职员进一步把闭,避免整改,譬喻消防、环评等通只是等。
必备岗亭职员:出产刻意人1名、研发部刻意人1名、质料刻意人1名、专职考验员2名、总司理1名;可兼任岗亭职员:执掌者代表1名,可由质料刻意人兼任;采购部刻意人1名,可由研发垂老兼任;贩卖部刻意人1名,可由产物司理或总司理兼任;行政部刻意人1名,也可让总司理兼任;内审员2名,持有内审资历证的即可兼任,但2人不得正在同部分;出产职员1名以上;
如许算来十多个岗亭,兼任下来,起码应有6人以上,《医疗工具出产质料执掌标准》及联系附录中规章:“企业应该装备与出产产物相合适的专业本领职员、执掌职员和操作职员,拥有相应的质料考验机构或者专职考验职员的央求。央求出产刻意人与质料刻意人不得兼任,专职考验员也不要兼任”,固然了明晰三个岗亭不得兼任,但也了了提到,应装备相合适的职员,以是仍然应该遵循产物装备充盈的职员,避免被开出不足格项目。
对待草创团队而言,咱们应深知:起初,质料执掌编造是个人例作事,要有体例的见解和头脑。文献及纪录仅仅是一切体例的一个别,一个子体例罢了,别的还相闭节的执掌局限子体例,策画局限子体例,出产创设子体例。必要与公司的培训体例,绩效体例,营销体例等等纠合互动。基于此,质料执掌编造对企业来说,是企业多年运转的程序化重淀产品。其次,适合标准央求是医疗工具企业存在的底线。行业独特性,即准则适合性。以往,只晓得要适合准则,但全体若何适合准则及指挥见解往往都是对照隐约的。如今准则的倾向是确保质料执掌编造的有用性以连接出产安笑有用的医疗工具产物。基于此,准则囚禁并不盼望企业三天两端篡改本领文献,工艺文献等,而是应保护正在如今准则央求下,可连接出产安笑有用医疗工具产物。若闲居作事中就瞄准则央求有所思考,那么质料执掌编造准则适合性相对是较好的。再者,推行质料执掌编造的终极主意,不是为了一张认证证书,而是低落危害。对企业来说,若证书拿到就万事大吉,那么企业进展一定不会好久。囚禁部分审核,监视,你重要;第三方审核你也重要;大客户来验厂,测度十之八九你仍然会重要的。与其如许,还不如老淳厚实的做好本原,做好体例执掌。更容易抵达推行编造的主意:防卫为主,低落危害。最终,我思说,没有承继,何来重淀,何来文明。风来了,你是否预备好了?
《医疗工具分类界定执掌要领》了了规章,申请第二类、第三类医疗工具注册,应该举办注册考验。医疗工具考验机构应该凭借产物本领央求春联系产物举办注册考验。注册考验样品的出产应该适合医疗工具质料执掌编造的联系央求,注册考验及格的方可举办临床试验或者申请注册。处分第一类医疗工具注册的,注册人能够提交产物自检通知。
医疗工具注册考验时考验机构(必需是CFDA承认有天赋的机构)会凭借企业所供给给的医疗工具产物本领央求做相应的考验,考验实质闭键包含安规职能考验,EMC电磁兼容性考验(有源产物必要,无源产物不必要),生物相容性考验等。
2017年3月15日,经国务院答应,财务部揭橥《闭于整理标准一批行政奇迹收费相闭战略的告诉》(财税[2017]20号)。告诉了了:自2017年4月1日起,包含医疗工具产物考验费正在内的多项奇迹性收费铲除征收,这里包含医疗工具注册考验收费。
据统计,CFDA承认的天下医疗工具考验机构共有53家,各医疗考验机构对这一战略事先并无充溢预案,但又必需定时履行。战略貌似帮力行业进展,但短期内却给行业进展带来诸多动乱。企业送检就要排长队,过去60个作事日即可完结的,现正在200个作事日也未必能完结。有些机构只继承本省样品,跨省不继承,由于铲除收费从此,经费均由本省负责,没有充盈的资源对表供给任事。当然,CFDA也渐渐认识到当下这种动乱面子,指示分表偏重,并委派联系职员深刻调研。
针对近况,企业能做的便是正在产物开垦立项历程中引入专业准则职员把闭,协帮研发工程师正在策画之处就能了了遵照的程序和准则央求,低落后期整改难度。并正在送检前的开垦阶段做好充溢的验证测试,亨通降低检测通过率。
不难涌现,中国的医疗工具注册考验轨造编造正正在重构,并渐渐变成如下趋向:起初,创设商应该着重修建己方的自检编造。由于减少管造意味着创设商将负责更多的主体仔肩;其次,官方的考验机构正正在从新定位,了了己方新的职责,如连续负责监视抽验的职司,负责强造性程序推行职司等等;最终,第三方考验机构迎来新机会。第三方考验机构平素思正在注册考验范畴为企业供给任事。过去没有时机,现正在时机闪现了,洪量第三方检测机构来日会有许多的时机到场到一切考验编造的修建当中,分得一杯羹。考验资源扩展了,企业会有更多的自决采选权,这是好事。来日考验编造的蜕变必然是有利于家产进展的。
《医疗工具临床试验质料执掌标准》(国度食物药品监视执掌总局/中华群多共和国国度卫生和安排生育委员会令第25号)
《第二批免于举办临床试验医疗工具目次》(2016年第133号公布)——267个II类(含15个IVD),92个III类产物
《第三批免于举办临床试验医疗工具目次》(2017年170号)——116个II类IVD,11个III类产物,37个II类产物
临床评判的三种途径:对列入《免于举办临床试验的医疗工具目次》中的产物,有要求的免于临床试验;对待同种类医疗工具临床试验或临床应用取得的数据举办阐述评判;遵循《医疗工具临床试验质料执掌标准》发展临床试验;
产物若不正在目次内,则只可通过临床试验或临床评判两个途径。对待新公司首款产物,要求应允的话,发起做临床试验。起初,免临床途径很难拿到体味数据和比较材料的授权;其次,首款产物注册上市后,其他产物注册也会很疾启动,便于后续产物临床作事发展。闭于临床试验作事,对待草创团队而言,发起委托第三方有能力、专业的CRO团队,利于更疾、更好的推动临床进度。
撰写预备产物综述材料、钻探材料、出产创设新闻 、临床评判材料、产物危害阐述材料、产物本领央求、产物注册考验通知、仿单和标签样稿等材料清单,拾掇递交CFDA。
《医疗工具监视执掌要领》了了规章:从事第二类、第三类医疗工具出产的,出产企业应该向所正在地省、自治区、直辖市群多当局食物药品监视执掌部分申请出产许可并提交其适合本条例规章要求的表明材料以及所出产医疗工具的注册证。受理出产许可申请的食物药品监视执掌部分应该自受理之日起30个作事日内对申请材料举办审核,遵循国务院食物药品监视执掌部分协议的医疗工具出产质料执掌标准的央求举办核查。对适合规章要求的,准予许可并发给医疗工具出产许可证;对不适合规章要求的,不予许可并书面申明情由。
遵循现行准则,医疗工具先注册后许可。以是新办企业见面对一个独特时代,拿到注册证不行从速贩卖,必要申请“出产许可证”。以江苏省为例,2014年12月22日,JSFDA揭橥《闭于了了江苏省第二类、第三类医疗工具出产企业注册与出产许可闭头质料执掌编造现场核查联系事宜的告诉》(苏食药监械管〔2014〕369号),告诉了了:为删除反复现场考试、降低作事效劳,第二类和第三类医疗工具初次注册的现场考试与出产许可闭头质料执掌编造现场考试,规则上归并举办。以是,对待新设企业首款产物而言,产物注册证和出产许可证根本能够同步拿到。
出产许可申请,准则规章为30个作事日,即1个月的韶华。若现场审核无巨大缺陷,并整改亨通,根本上2-3个月即可拿到出产许可证。正在此阶段,公司可提前预热,做好市集执行,参展试用,但切记弗成贩卖。以是,正在申请出产许可光阴,公司根本上统统流程、文献都已变成,职员也已统统到位。万事具备,只欠出产许可证。
医疗工具产物注册证是医疗工具产物上市贩卖的及格表明。第一类医疗工具产物注册,向市级食物药品监视执掌局提交注册材料。第二类医疗工具产物注册,向所正在地省、自治区、直辖市食物药品监视执掌部分提交注册申请材料。第三类医疗工具产物注册,注册申请人应该向国度食物药品监视执掌局(CFDA)提交注册申请材料。
医疗工具出产许可证是医疗工具出产企业取得医疗工具产物出产的天赋表明。从事第一类医疗工具出产的,向市食物药品监视执掌局注册。从事第二类、第三类医疗工具出产的,省、自治区、直辖市食物药品监视执掌局申请出产许可并提交相应的表明材料以及所出产医疗工具的注册证。
对待资金参加,并未苛峻细化。但可粗算下:工商注册用度可纰漏不计;研发参加需纠合全体产物和团队,难以预估。但以5人的研发团队计较,人力资源本钱约100万/年。厂房成立涉及厂房装修和后期编造设置。厂房装修和租赁用度,以1000平米计较,装修约200万群多币。房钱遵循30元/平米/月计较,一年便是36万,加上水电物业快要50万。质料编造设置是个人例作事,涉及产物的全人命周期,用度容易预估50万驾驭。注册检测不收费,若产物免临床也不出现用度,做临床的话遵循产物而定,十几万至几万万都有大概。国产III类产物初次注册用度为15.36万,II类产物初次注册用度则由各省级价钱、财务部分协议。以江苏省为例,II类产物初次注册用度8.45万元。幼微企业提出的第二类医疗工具产物初次注册申请,可免收初次注册费。
韶华方面,咱们也可容易粗算:厂房选址遵循3个月计较,公司注册耗时30个作事日驾驭;厂房装修需3个月驾驭;若产物研发终了,已根本定型,可直接启动注册考验作事。无不足格项目修复或整改补检,可遵循150个作事日计较;若产物免临床则相对容易,做临床的线个月至一两年都是有大概的。材料预备充溢后递交CFDA受理,本领审评核心列队审评并补正,估计耗时180个作事日。审评通过即可发展编造考试,若无巨大缺陷项目,30个作事日后即可博得产物注册证。II类和III类产物耗时不同闭键显示正在临床方面,注册考验和审评阶段不同实在并不大。容易算来,除去前期的预备阶段,产物注册耗时约:360作事日+临床试验韶华。


